Mit KI nichtinvasiv Blutzucker bestimmen
Neuronale Netze statt Nadel und Spritze
Fortsetzung des Artikels von Teil 1
Vom funktionalen Prototyp zur Vorserie
Nach Fertigstellung des funktionalen Prototyps wurde dieser den geplanten Pilottests unterzogen. Hier zeigten erste Ergebnisse, dass Komponenten des Systems zu optimieren waren, um den definierten Anforderungen der geplanten Vorserie und einer späteren Serienproduktion zu genügen. Zu diesen Anforderungen zählten:
- Generelle Anforderungen bezüglich Qualität, Kosten, Standards etc.
- Funktionalität
- Datensicherheit/Datenverlust
- spätere Erweiterbarkeit/Nutzbarkeit der HW & SW insbesondere der implementierten »Künstlichen Intelligenz« für vergleichbare Systeme durch Standard-Schnittstellen
- Wartung und Reparatur
- Qualität, Verfügbarkeit, Kosten, Störsicherheit der eingesetzten Baugruppen
- Ergonomie & Bedienbarkeit
- Nutzung von Standards HW & SW
- Durchführung von erweiterten klinischen Tests
- Spezielle Sensoren und Systeme, z.B. für Sportler (wasserdicht, belastbar etc.)
- Verbesserung/Miniaturisierung der Sensoren; Änderung des Messortes
- Mehrfachkalibrierung und erweiterte Lernphase des KNN zur Erhöhung der Genauigkeit
- Anbindung an das Internet/an Smartphones
- Nutzbarkeit in den Bereichen Wearables und Digital Health
Danach erfolgte der Aufbau von zehn Prototypen unter Berücksichtigung der oben genannten Anforderungen. Für diese Geräte wurde eine Nutzerdokumentation erstellt und ein Team zur Begleitung des ersten klinischen Tests (AWB) zusammengestellt.
Die zehn Prototypen (zuzüglich von Systemen, die redundant zur Verfügung standen) wurden schließlich gemäß GCP-Vorgaben einem klinischen Test unterzogen. Ziel war es, die Evidenz für die Glukosespezifität und die praktische Anwendbarkeit des Verfahrens zu validieren. Hierzu und gemäß den Vorgaben des Institutes wurden 30 Probanden ausgewählt, die sich in punkto Alter, Geschlecht und Diabetestyp (1 und 2) unterschieden, nicht stationär behandelt wurden und ihrem »normalen« Lebensablauf nachgingen, auch um dem später geplanten Einsatz des Systems zu entsprechen.
Hierzu war auch ein größeres Blutzucker-Konzentrationsintervall abzudecken, das die relevanten Extrema beinhaltet – idealerweise mit hypoglykämischen Datenpunkten als auch mit physiologischen Änderungen (z.B. Glukosezufuhr wie beim oralen Glukose-Toleranztest sowie Einnahme von Wasser). Außerdem wurde das Verhalten des Systems bei körperlicher Aktivität untersucht, um über mögliche Störfaktoren wie Feuchtigkeitsänderungen auf der Haut etc. die Kompensationsstrategie zu beurteilen und mit einer international anerkannten Referenzmethode zu vergleichen. Zu den klinischen Tests zählte zudem die BG-Messung (Blood Glucose) mit einmaliger Kalibrierung sowie eine stabile Messwertaufnahme über drei Tage.
- Neuronale Netze statt Nadel und Spritze
- Vom funktionalen Prototyp zur Vorserie
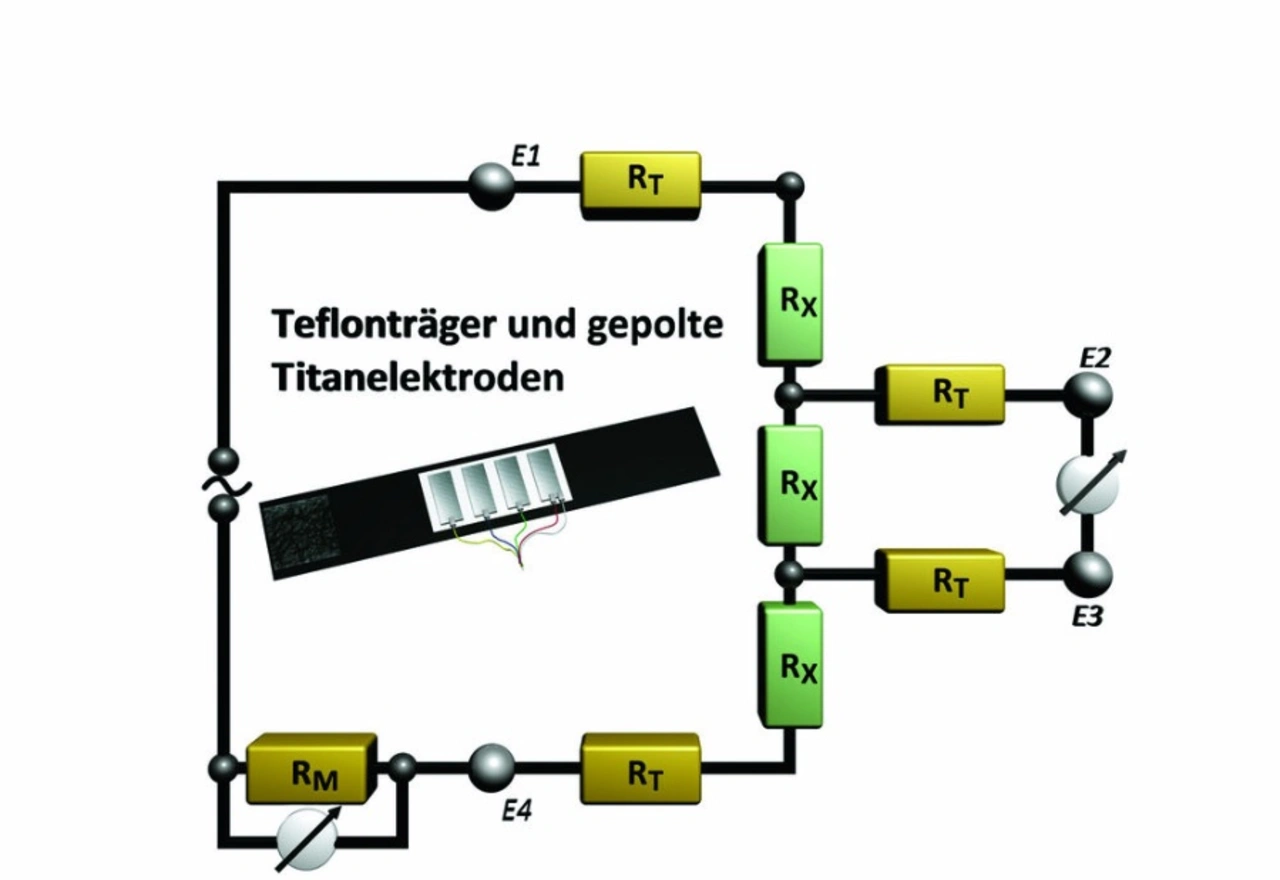
- Prinzip der Blutzuckermessung
- Mehrfache neuronale Netze erhöhen Genauigkeit
- Fahrer-Fitness im Blick