KI in der Radiologie
Ich sehe was, was du nicht siehst
Fortsetzung des Artikels von Teil 1
Beschleunigte Diagnose
Was nach Zukunftsmusik klingt, steht schon mit einem Bein in der Tür der Medizin. Das ist auch dringend nötig. Allein die Datenmengen haben eine Größenordnung erreicht, die sich ohne KI nicht mehr verwalten lässt, wie zum Beispiel die Auswertung zehntausender MRT-Scans. »Intelligente Algorithmen sorgen für Verbesserungen in puncto Genauigkeit, Schnelligkeit und Automatisierung«, sagt Dr. Michael Graß, Chefwissenschaftler bei Philips Research. Ein gut eingespieltes Team aus Mensch und Maschine könne eine höhere Qualität und Effizienz erzielen. »Das kommt dem Radiologen, dem Patienten und letztlich dem gesamten Gesundheitssystem zugute.«
Mit der neuesten Generation von Kernspintomografen lassen sich die Messzeiten deutlich reduzieren. Ein Beispiel dafür ist das Ingenia Elition 3.0T von Philips (Bild 1). Das System wurde nicht nur unter Berücksichtigung von Patientengesichtspunkten in seiner Architektur verbessert, sondern nutzt auch Technologien, die sich der KI bedienen. Eine dieser Technologien ist »Compressed Sense«. Mit ihr lassen sich nicht nur die Sequenzen, sondern die gesamte Untersuchung beschleunigen. 2D- und 3D-Scans aller anatomischen Kontraste und Körperbereiche sollen mit nahezu gleicher Bildqualität um bis zu 50 % beschleunigt werden. Alternativ könne das Beschleunigungsverfahren auch genutzt werden, um in gleicher Zeit eine höhere Auflösung zu erzielen und so Läsionen bei Multipler Sklerose besser zu erkennen oder Hirntumoren genauer differenzialdiagnostisch zu unterscheiden (Bild 2). Im Bereich Multiple Sklerose sei es auch möglich, ein komplettes Protokoll ohne Kontrastmittel unter zehn Minuten bei gleichbleibender Bildqualität durchzuführen. »Wir erhalten die gleichen Informationen, und die Diagnostik wird für den Patienten angenehmer, zuverlässiger und schneller«, sagt Dr. Jan Kirschke, Abteilung für Diagnostische und Interventionelle Neuroradiologie am Klinikum rechts der Isar der Technischen Universität München. Zudem verfügt das volldigitale MRT-System mit »VitalEye« über eine KI-basierte Detektionstechnologie, die den Scan auf den Atemzyklus des Patienten abstimmt. Neben der laufenden Überprüfung von Atmung und Atemmuster lässt sich auch das Auslösen von Atemtriggerung darüber steuern.
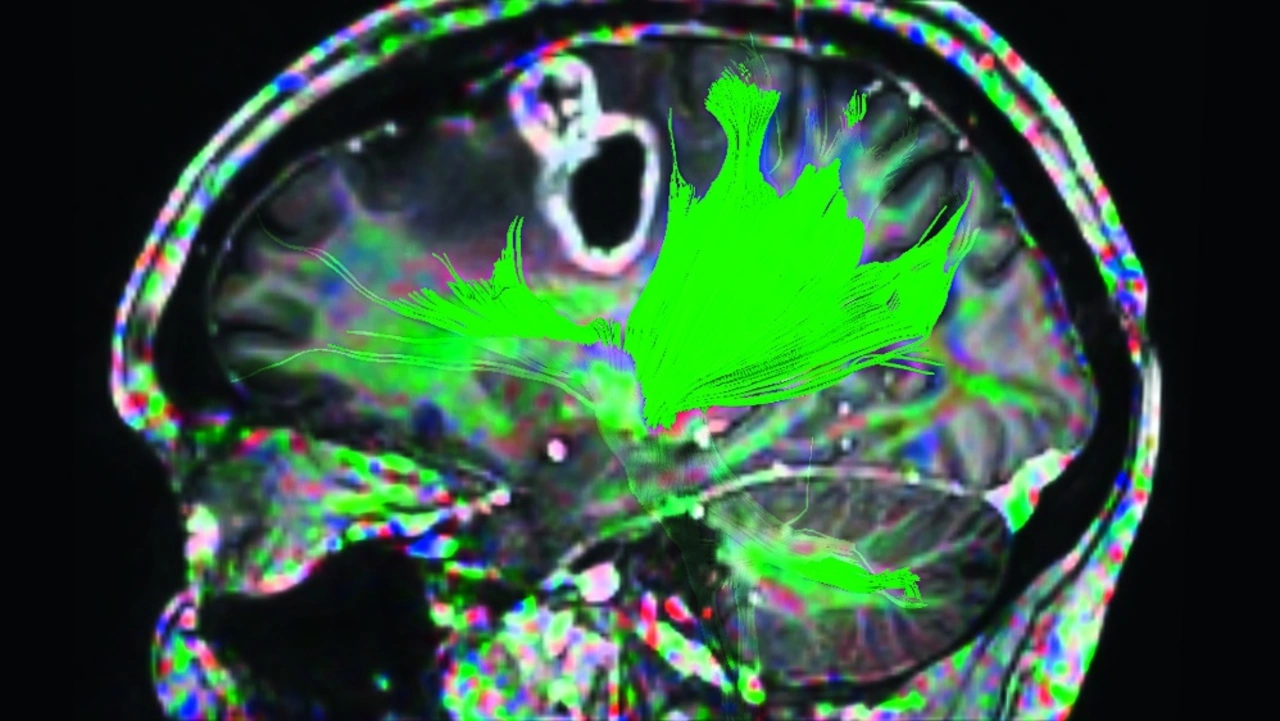
Tiefer Blick
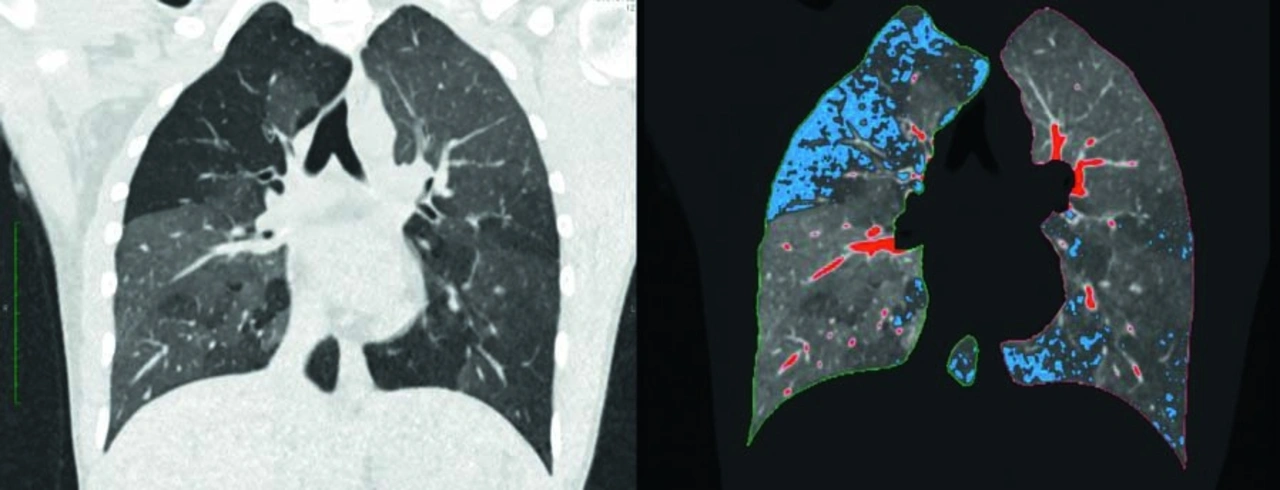
»Wenn wir uns als Radiologen CT-Bilder ansehen, dann sehen wir helle und dunklere Areale und beurteilen das Organ anhand dieser Helligkeitsunterschiede«, sagt Joshua Gawlitza vom Institut für klinische Radiologie und Nuklearmedizin der Universitätsmedizin Mannheim. Auch Software-Programme, von denen sich Radiologen schon seit Längerem bei der Auswertung einer CT helfen lassen, werten in der Regel Dichteunterschiede auf den Aufnahmen aus und ermitteln in den jeweils interessierenden Regionen Durchschnittswerte. Dabei lassen sich den umfangreichen Datensätzen moderner CT-Geräte auch ganz andere Auswertungen machen. Ein Beispiel dafür ist die quantitative Computertomografie (qCT). »Bei diesem Verfahren wertet die Software nicht nur durchschnittliche Dichtewerte aus, sondern analysiert jeden einzelnen dreidimensionalen Pixel oder Voxel separat und setzt sie miteinander in Verbindung«, erläutert Gawlitza. In der Lunge beispielsweise wertet die qCT pro Lungenflügel mehr als zwei Millionen Voxel aus. Bei Patienten mit einer chronisch-obstruktiven Lungenerkrankung (COPD) ist die Lunge nicht homogen belüftet. Es gibt vielmehr Areale, in denen die Luft beim Ausatmen »steckenbleibt« und andere, die weitgehend normal arbeiten. Solche schlecht belüfteten Areale lassen sich mit der qCT gut erkennen (Bild 3). Ein anderes Beispiel sind Verkalkungen der Herzkranzgefäße, die in der normalen CT ohne Quantifizierung lediglich als dichte Ablagerungen erscheinen. In der qCT dagegen kann der Aufbau der Kalk-Plaques sowie deren Volumen detailliert dargestellt und vor allem quantifiziert werden. Insbesondere für die individuelle Risikoabschätzung des Patienten ist dies relevant.
In einer Studie untersuchten Gawlitza und sein Team, ob aus den sehr detaillierten Informationen, die die qCT liefert, nicht auch Rückschlüsse auf die Funktion der Lunge gezogen werden können. Konkret haben die Mannheimer mehrere qCT-Parameter – darunter Lungenvolumen, mittlere Lungendichte und den Anteil der schlecht belüfteten Lungenareale – in ein neuronales Netzwerk gefüttert. Zum Einsatz kam das dafür in Mannheim eigens für die qCT-Auswertung der Lunge entwickelte Programm »PrediCT«. »Letztlich rechnet die Software die Lungenfunktion auf Basis unterschiedlicher Modelle durch und bildet einen Mittelwert. Den haben wir dann mit dem Goldstandard, einer Messung der Lungenfunktion mittels Bodyplethysmografie, verglichen«, so Gawlitza. Um etwa zehn Prozent weichen die von der Software berechneten Lungenfunktionsparameter von jenen ab, die per Goldstandard-Methode gemessen wurden [4].
Meilensteine der medizinischen Bildgebung1895: Eine neue Art von Strahlen Eher zufällig entdeckt Conrad Röntgen am 8. November 1895 die nach ihm benannten Röntgenstrahlen. Bereits drei Monate danach wird Siemens das Patent auf »Eine neue Röntgenlampe mit regulierbarem Vakuum« erteilt, mit der sich der gesamte Körper erwachsener Persönen durchleuchten lässt. 1927: Blick in die weibliche Brust Der Chirurg Otto Kleinschmidt führt am Universitätsklinikum in Leipzig die weltweit erste klinische Mammographie an einer Patientin durch. Es ist der Beginn der präoperativen Mammographie, die heute zur Routineuntersuchung vor einer Brustoperation gehört 1972: Das Gehirn wird sichtbar Nach Vorarbeiten des Physikers Allan M.Cormack realisiert der Elektrotechniker 1971 Godfrey Hounsfield mehrere Prototypen von CT-Geräten. Bereits ein Jahr später führt er die erste klinische Gehirnuntersuchung mittels Computertomographie durch. 1977: Der gläserne Patient Raymond Damadian gelingt die erste MRT-Aufnahme des menschlichen Körpers – ein Thoraxquerschnitt. Obwohl das Bild technisch sensationell ist, reicht die Ortsauflösung bei weitem nicht für eine diagnostische Verwendung. Die Aufnahmezeiten betragen mehrere Stunden und sind damit für eine praktische Anwendung viel zu lang. 2017: Neue Wege bei der Brustkrebserkennung US-Wissenschaftler entwickeln ein Programm, das unter auffälligen Gewebeveränderungen in der Brust diejenigen erkennt, die sich im weiteren Verlauf zu Krebs entwickeln. So sollen zukünftig unnötige Biopsien und Operationen vermieden werden. 2018: Maschine schlägt Mensch Bei einem Versuch mit 100 Bildern von bösartigen Melanomen und gutartigen Muttermalen stellt ein Computerprogramm im Durchschnitt häufiger die richtige Diagnose als 58 Hautärzte aus verschiedenen Ländern. Die Forschergruppe um Holger Hänßle von der Universität Heidelberg verwendet für ihre Untersuchung ein CNN. |
KI unterstüzt Ärzte bei der Diagnose
Die Beispiele zeigen: Künstliche Intelligenz und neuronale Netzwerke sind wichtige Werkzeuge für die Radiologie, die oft auch das sehen, was das menschliche Auge nicht sieht. Selbstlernende Algorithmen können verborgene Muster in den Daten aufspüren und den Medizinern wertvolle Unterstützung für ihre Diagnose- und Therapieentscheidungen geben. »Wenn es um das Erkennen relevanter Muster und Zusammenhänge in komplexen Datenmengen geht, sind Computer mittlerweile besser als der Mensch«, sagt Horst Hahn vom Fraunhofer-Institut für Bildgestützte Medizin MEVIS. Das bedeute aber nicht, dass der Rechner die Therapieentscheidung trifft, sondern er unterstützt die Ärzte durch sein datenbankbasiertes Wissen.
Auch der Essener Michael Forsting sieht die Entwicklung positiv und glaubt nicht, dass Radiologen durch KI verdrängt werden. »Klar wird es weiterhin Radiologen geben! Wir müssen nur vielleicht nicht mehr die langweiligen Sachen machen, Mammografie- und Lungenscreening zum Beispiel.« Die Diskussion um den Einsatz dürfe nicht über Rationalisierungsängste geführt werden, sondern es muss um Qualität gehen. »Und wenn künstliche Intelligenz die Qualität der Radiologie verbessert – wovon ich überzeugt bin – dann wird sie sich in den Gesundheitssystemen durchsetzen.«
Quellen
[1] T. Franke: Macht künstliche Intelligenz Ärzte überflüssig?, https://www.beipress.de/2016/09/21/macht-kuenstliche-intelligenz-aerzte-ueberfluessig/ (04.06.2018)
[2] A. Conner-Simons: Using artificial intelligence to improve early breast cancer detection, http://news.mit.edu/2017/artificial-intelligence-early-breast-cancer-detection-1017 (04.06.2018)
[3] D. Ribli u.a.: Detecting and classifying lesions in mammograms with Deep Learning, https://www.nature.com/articles/s41598-018-22437-z (04.06.2018)
[4] N. Keil: Neuronales Netz blickt tief in die Lunge, https://www.drg.de/de-DE/4254/neuronales-netz/ (04.06.2018)
| Zuerst gesehen: Dieser Beitrag stammt aus der Medizin+elektronik Nr. 4 vom 20.07.2018. Hier geht’s zur vollständigen Ausgabe. |
|---|
- Ich sehe was, was du nicht siehst
- Beschleunigte Diagnose