Agile Entwicklungsmethoden
Level up: So entsteht Software schneller
Fortsetzung des Artikels von Teil 1
Warum überhaupt auf agile Entwicklung setzen?
Bei der agilen Methode müssen bei Projektstart die Anforderungen noch nicht vollständig bis ins Detail definiert sein. Das unterscheidet sie von traditionellen Methoden, die vollständig definierte Leistungsanforderungen verlangen. Somit kann bei der agilen Software-Entwicklung der tatsächliche Entwicklungsprozess deutlich früher beginnen, ohne eine unnötige Fixierung auf Details, die sich im späteren Verlauf möglicherweise aus praktischen Gründen oder aufgrund von falsch verstandenen Anforderungen als irrelevant erweisen.
Agile Herangehensweisen ermöglichen es zudem, medizintechnische Produkte und deren Software-Komponenten frühzeitig ersten Praxistests zu unterziehen. Die in kurzen Abständen durchgeführten Planungs- und Entwicklungszyklen erleichtern den regelmäßigen Abgleich der Softwareentwicklung mit den Anforderungen von Nutzern. Ist das Produkt beispielsweise stark kundenorientiert und ändern sich Anforderungen immer wieder, verlangt dies höchste Flexibilität bei den Entwicklern. Agile Methoden helfen dabei, die veränderten Kundenwünsche in den Entstehungsprozess einfließen zu lassen.
Agile Entwicklung mit Vorschriften abgleichen
Die für die Produktentwicklung relevante Norm IEC 62304 schreibt ein V-Modell für die Software-Entstehung vor. Die Norm soll sicherstellen, dass die allgemeinen Anforderungen an die medizinische Softwareentwicklung erfüllt werden und die vorgeschriebenen Prozesse kontrolliert ablaufen. Mit den im V-Modell beschriebenen Arbeitsschritten wird ein kontinuierlicher Fortschritt erzielt, bis das Produkt fertiggestellt ist.
V bedeutet mehr Freiheit
Häufig wird bei dem V-Modell angenommen, dass die Aktivitäten sequenziell ablaufen müssen, dass also eine Phase beendet sein muss, bevor mit der nächsten Phase begonnen wird. Tatsächlich beschreibt das V-Modell nur die Abhängigkeit zwischen Aktivitäten, nicht aber ihre Reihenfolge. Diese Freiheit lässt sich nutzen, um auf Ebene der Arbeitsorganisation das V-Modell in die agile Methodik zu überführen.
Dies ist möglich, da der Gesetzgeber nicht die anzuwendenden Prozesse vorschreibt. Vielmehr wird eine Reihe von Aktivitäten definiert, die ein Unternehmen im Rahmen seiner Prozesse ausführen sollte. Den Herstellern ist es dann überlassen, wie diese Aktivitäten im Zeitverlauf umgesetzt werden. Verpflichtende Meilensteine wie der Abgleich von Anforderungen mit dem Funktionsumfang sowie die Verifizierung von Input und Output stellen sicher, dass die Vorschriften eingehalten werden.
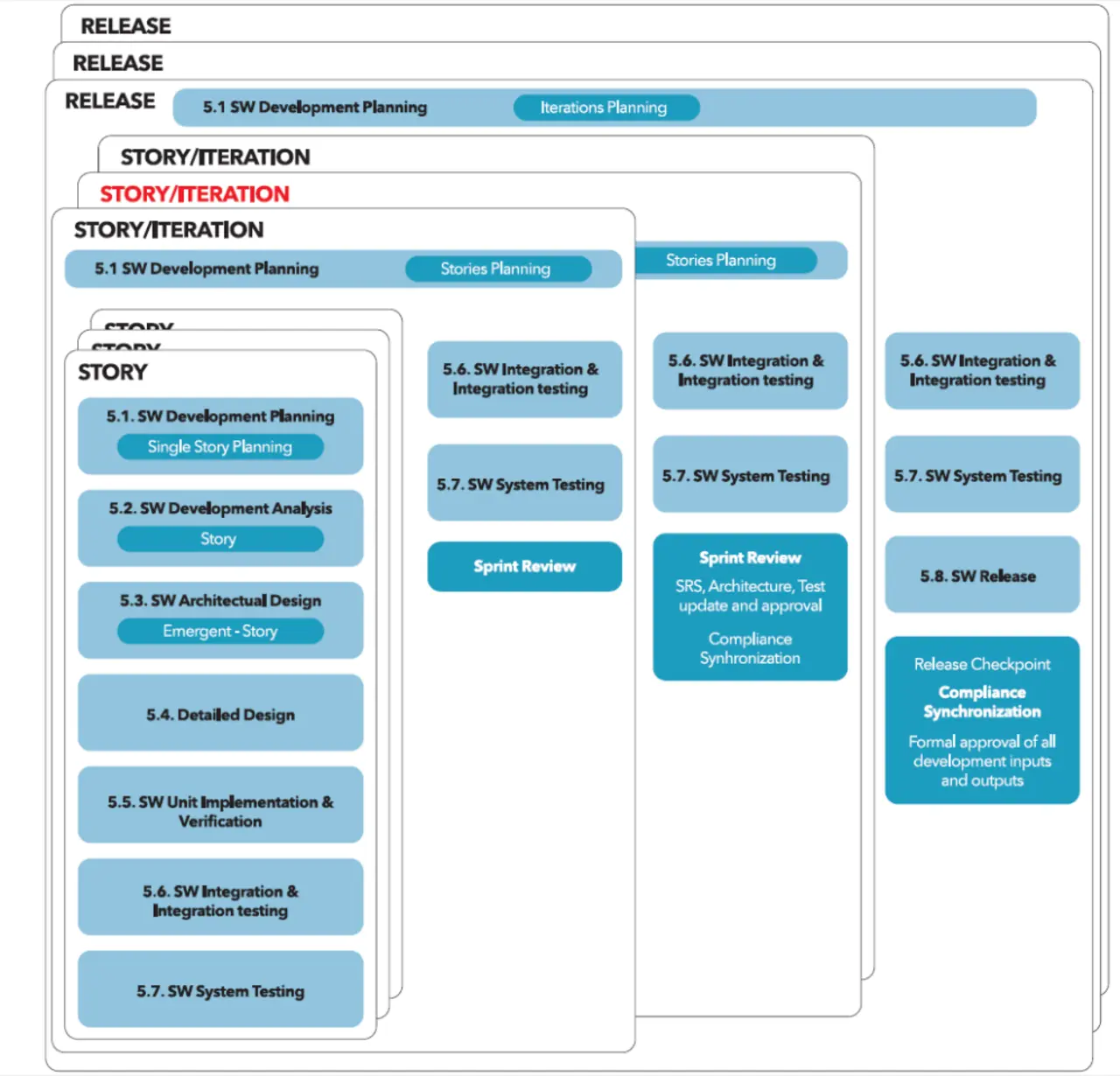
 |
Pflichtelemente des Software-Entwicklungsprozesses für Medizingeräte |
Umsetzung in der Praxis
Leider gibt kein universelles Erfolgsrezept zur Einführung der agilen Entwicklungsmethode. In der Praxis hat es sich jedoch als sinnvoll erwiesen, die anfallenden Aufgaben und Abläufe in mehrere Ebenen zu strukturieren. Grundlegende Prozesse auf hoher Ebene sollten in einem zentralen Quality-Management-System (QMS) definiert werden. Detaillierte Abläufe, wie der Software Development Life Cycle (SDLC), die genutzten Werkzeuge und Technologien, werden im Qualitätsplan des Projekts festgehalten. So ist weiterhin eine flexible Gestaltung bei der Umsetzung möglich und der Projektleiter kann Prozesse speziell auf die Bedürfnisse eines Kunden oder Unternehmens abstimmen. Hier lassen sich die Projektumstände wie Benutzerinteraktion, Klarheit der Anforderungen, Zeit- und Budgetbeschränkungen oder Markteinführungszeit im Detail berücksichtigten.
Passende Tools auswählen
Ständige Iterationen, bei denen sich alle Artefakte ändern und weiterentwickeln, sorgen dafür, dass das Team die Dokumentation konsistent und jeweils auf dem neuesten Stand hält. Hierfür sind entsprechende Werkzeuge notwendig, um die Nachverfolgbarkeit von Anforderungen, Architektur, Design, Implementierung und Tests zu garantieren sowie Änderungen zu steuern. Unternehmen sollten daher ein Werkzeug für das Application Lifecycle Management (ALM) zu einem integralen Bestandteil für die Einhaltung der gesetzlichen Anforderungen machen.
Fazit
Die agile Softwareentwicklung für Medizinprodukte lässt sich mit den Forderungen der IEC 62304 in Einklang bringen. Es kommt nur darauf an, die Abläufe innerhalb der Entwicklungsabteilung so zu organisieren, dass die zentralen Anforderungen der Vorschriften erfüllt werden. So gelingen die Verifizierung und Validierung, das Risikomanagement sowie die Nachverfolgbarkeit der Software-Komponenten exakt in der Form, wie dies der Gesetzgeber vorsieht. Gleichzeitig gewinnt die Produktentwicklung an Geschwindigkeit, während die Produktqualität steigt und eine verbesserte Innovationsfähigkeit die eigene Marktposition festigt.
| Link-Tipp |
|---|
Ein Whitepaper von Comtrade Digital Services informiert ausführlich über die agile Software-Entwicklung in der Medizintechnik. Dies ist kostenfrei abrufbar unter: http://content.comtradedigital.com/ |
*Bild: “Phasen des V-Modells über Zeit und Detaillierung“ von Michael Pätzold. Lizenz: CC-BY-SA 3.0
- Level up: So entsteht Software schneller
- Warum überhaupt auf agile Entwicklung setzen?