Durchflusszytometrie und KI
Smarte Laser-Lichtschranke für Krebszellen
Fortsetzung des Artikels von Teil 1
Bewertung von Machine-Learning-Algorithmen
Ein wesentlicher Vorteil von Matlab ist die Möglichkeit, zahlreiche unterschiedliche Machine-Learning-Modelle in kurzer Zeit zu testen. Das Team von der UCLA verglich vier Klassifikationsalgorithmen aus der Statistics and Machine Learning Toolbox: naive Bayes-Klassifikation, Support Vector Machine (SVM), logistische Regression (LR) und ein tiefes neuronales Netz (Deep Neural Network, DNN), das mit Kreuzentropie und Backpropagation trainiert wurde.
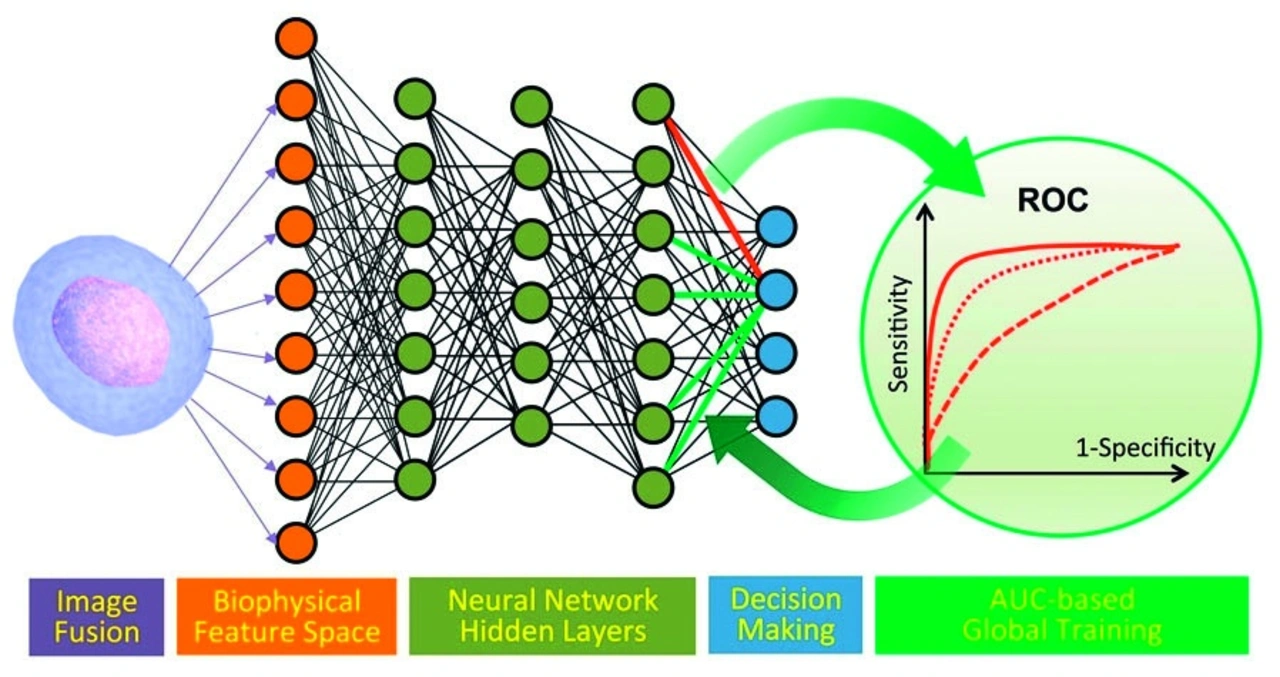
Bei Tests von Stichproben mit bekannter ZTZ-Konzentration (Zirkulierende Tumorzellen, ZTZ) erreichten alle vier Algorithmen eine Genauigkeit von über 85 Prozent (Bild 1). Die Genauigkeit, die Konsistenz und die Balance zwischen Sensitivität und Falsch-Positiv-Rate der Machine-Learning-Klassifikation ließen sich weiter verbessern, indem Deep Learning mit einer globalen Optimierung der Receiver Operating Characteristics (ROC) kombiniert wurde. Nach der Implementierung erhöhte sich die Klassifikationsgenauigkeit dank des neuen Ansatzes auf 95,5 Prozent.
Aufgrund der gigantischen Datenmengen benötigte das Team häufig mehr als eine Woche, um seine Bildverarbeitungs- und Machine-Learning-Prozesse abzuschließen. Die Ausführzeiten konnten sie jedoch mithilfe eines 16-Core-Prozessors und der Parallel Computing Toolbox verkürzen. Dank einer einfachen parallelen For-Schleife (parfor) führten sie die Prozesse gleichzeitig auf den 16 Prozessoren aus und verringerten den Zeitaufwand für die Analyse von acht Tagen auf circa einen halben Tag.
Modellieren des Versuchsaufbaus
Im Photoniklabor der UCLA ist Matlab das Haupt-Arbeitstool für die Modellentwicklung und die Datenanalyse. Das Projektteam verwendete die Software, um ein Modell des gesamten Versuchsaufbaus zu entwickeln, von den optischen Geräten und den Laserimpulsen bis hin zur Klassifikation einzelner Zellen (Bild 2). Dieses Modell diente als Grundlage, um den Versuchsaufbau zu verbessern – beispielsweise das Signal-Rausch-Verhältnis. Dafür verwendete das Team das Modell zur Simulation spezifischer Laserverstärkungs-Koeffizienten. Die Ergebnisse zeigten, wie und wo Veränderungen des Aufbaus die Gesamtleistung verbessern konnten.
Indem sie das System in Matlab modelliert und simuliert haben, konnten die Forscher Monate für Experimente sparen und gewannen dabei außerdem eine Grundlage für die nächsten Schritte. Zurzeit integrieren sie detaillierte Modelle einzelner Zellen in das Modell des Gesamtsystems, mit denen sie in der Lage sind, fundiertere Kompromisse zwischen der räumlichen Auflösung und der Phasenauflösung einzugehen.
Das System kann jedoch nicht nur Krebszellen klassifizieren. Es kann auch verwendet werden, um Zellen von Algen anhand ihres Fettanteils und ihrer Eignung als Biokraftstoffe zu klassifizieren. Die einzige wesentliche Veränderung, die dafür vorgenommen werden müssen, betrifft die Oberflächenbeschichtung in dem Kanal, durch den die Zellen fließen. Unverändert bleibt die der Analyse zugrunde liegende Machine-Learning-Pipeline (Bild 3). Sie lernt eigenständig, dass für die Klassifikation von Algenzellen Merkmale optischer Verluste und Phasen wichtiger sind als morphologische Merkmale, während für Krebszellen genau das Gegenteil der Fall ist.
| Kurz erklärt |
|---|
Die Durchflusszytometrie ist ein leistungsstarkes Verfahren für die schnelle Messung mehrerer Eigenschaften einzelner Partikel, die sich durch ein strömungstechnisches System bewegen. Dazu gehören: relative Größe, Granularität, Komplexität sowie Fluoreszenzintensität. Bei den Partikeln handelt es sich meist um Zellen, möglich sind aber auch Bakterien und Beads . Das Messverfahren kommt sowohl in der Grundlagenforschung als auch in der klinischen Forschung, der Biotechnologie, der Toxikologie sowie im Bereich der Lebensmittelwissenschaft zum Einsatz. In der Grundlagenforschung wird die Durchflusszytometrie zur Bewertung der Expression verschiedener oberflächlicher oder intrazellulärer Moleküle beziehungsweise zellulären Gesundheit sowie zur Weganalyse eingesetzt. Klinische Forscher hingegen versuchen damit, Krankheitsmechanismen zu identifizieren sowie die Wirksamkeit von Medikamenten zu überprüfen. Bioingenieure nutzen die Durchflusszytometrie, um die Leistung von Biopolymeren als Transportvehikel für Medikamente zu untersuchen. Und in der Toxikologie lassen sich mit dem Verfahren die Auswirkungen von Chemikalien auf die Umwelt und im Lebensmittelbereich das Wachstum von Hefen während der Gärung analysieren. Grundsätzlich besteht ein Durchflusszytometer aus einem Flüssigkeitssystem, einem optischen sowie einem elektronischen System. Das Flüssigkeitssystem bringt die Probe über die Laserlichtquelle in den Anregungsweg und nutzt dabei entweder die hochdynamische Fokussierung oder die Kapillarströmung. Sobald die Proben die Laserlichtquelle passieren, erfolgt die Auswertung von Streuung und Fluoreszenz. Die Fluoreszenzdetektion erfolgt mit einer Reihe von Filtern in Kombination mit Photomultiplierröhren, Photodioden oder einem CCD-Array. Schließlich wird das resultierende Streu-/Fluoreszenzlicht zum elektronischen System geleitet und dort in elektronische Signale zur Analyse durch den Forscher umgewandelt. Merck bietet für Durchflusszytometrie unter anderem den Muse Cell Analyzer und den Ueva easyCyte an. Bei beiden handelt es sich um Geräte für den Labortisch, die die Vorteile einer mikrokapillaren Durchflusszelle mit einem robusten und zuverlässigen Gerätedesign kombinieren. Mit dem CellStream ist es dem Unternehmen gelungen, die Zellanalyse weiter zu optimieren. Ausgestattet mit sieben Lasern ermöglicht das Gerät die Nutzung von bis zu 22 Erkennungskanälen. Und schließlich verbinden die Serien Amnis FlowSight und Image Stream die Durchflusszytometrie mit der Fluoreszenzmikroskopie. |
* Claire Lifan Chen (Senior Application Engineer bei Lumentum Operations LLC); * Ata Mahjoubfar (Postdoktorand an der UCLA)
| Dieser Beitrag stammt aus der Medizin+elektronik Nr. 5 vom 10.09.2018. Hier geht’s zur vollständigen Ausgabe. |
- Smarte Laser-Lichtschranke für Krebszellen
- Bewertung von Machine-Learning-Algorithmen